ГЛАВА 3. Физико-химические основы процессов взаимодействия активных частиц плазмы с поверхностью
6. Закономерности и особенности взаимодействия плазмы галогенсодержащих газов с металлами и полупроводниками
Основные сведения по травлению материалов в галогенсодержащей ННГП приведены в обзорных статьях [9 – 12] и монографиях [1 – 3, 6, 8] и могут быть обобщены в виде следующих положений (см. также табл. 3.6.1):
- Для широкого круга металлов (Cu, Al, W, Mo, Ta, Nb) и полупроводников (Si, GaAs и др. соединения группы А3В5), основными химически активными частицами, обеспечивающими травление, являются атомы галогенов, образующиеся в плазме при диссоциации молекул плазмообразующего газа. Некоторым исключением здесь является медь, которая способна взаимодействовать как с атомарным, так и с молекулярным хлором в чисто термических условиях, без разряда. Скорости плазменного травления и термического хлорирования меди при одинаковых температурах образца близки, что косвенно свидетельствует о близких вероятностях взаимодействия для атомарного и молекулярного хлора.
- Многие металлы и полупроводники при взаимодействии с атомами галогенов образуют ненасыщенные галогениды, которые, однако, не всегда обладают достаточно высокой летучестью при температурах, близких к комнатной или обеспечиваемых нагревом материала за счет разряда. В последнем случае для эффективного проведения процесса травления необходима активация десорбции продуктов с поверхности (дополнительный нагрев, ионная бомбардировка, УФ излучение).
- Для большинства материалов, перечисленных в п.1, в широком диапазоне внешних параметров плазмы (Р = 1¸100 Па, Wуд = 0.01¸10 Вт/см3) реакция травления протекает в стационарной области, в кинетическом режиме и имеет первый кинетический порядок по концентрации химически активных частиц в газовой фазе. В условиях, когда доминирующим механизмом травления является химическая реакция (образование летучих продуктов взаимодействия и/или термическая активация десорбции), зависимости скорости травления от внешних параметров разряда удовлетворительно согласуются с их влиянием на концентрацию ХАЧ в объеме плазмы и величину плотности потока атомов на поверхность обрабатываемого материала.
- При проведении процесса в кинетическом режиме температурные зависимости скорости и вероятности взаимодействия подчиняются закону Аррениуса.
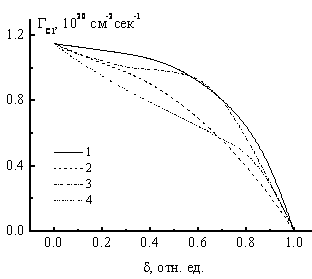
Вопросом, представляющим значительный интерес, являются процессы травления металлов и полупроводников в бинарных газовых смесях, где один из компонентов является «активным» (например, хлор или фторсодержащий газ), а другой – инертным (Ar, He) или молекулярным газом (N2, O2, H2). Для таких систем имеется большое число экспериментальных свидетельств немонотонного поведения скоростей травления различных материалов при изменении состава смеси в рамках постоянства общего давления и мощности, вкладываемой в разряд. Реальное количество примеров здесь очень велико, поэтому приведем лишь некоторые из них: Si, GaN, GaAs (рис. 1) и GaSb , InP и InSb , ZnS, (Ba, Sr)TiO3, (Pb, Zr)TiO3, TiO2, Pt и Cu (рис. 2) в плазме смеси Cl2/Ar; поли-Si, RuO2 и W в плазме смеси Cl2/O2, GaAs (рис.1) в плазме смесeй Cl2/N2 и Cl2/H2.
Для систем, представленных на рис. 1 и 2, зависимость скорости взаимодействия от внешних параметров разряда при фиксированном составе смеси отвечает закономерностям, найденным для плазмы чистого хлора. В то же время, варьирование начального состава смесей вызывает немонотонные – с максимумом – изменения скоростей травления, при этом скорость травления в максимуме в 1.5 – 3 раза превышает скорость травления в чистом хлоре. Для меди этот эффект наблюдается только при плазменном травлении, в условиях газового травления скорость падает пропорционально доле Cl2 в смеси. Очевидно, что отмеченный эффект имеет большие технологические перспективы, так как позволяет проводить процесс травления в условиях сильного разбавления хлора газом-добавкой практически без потерь в скорости процесса. В качестве причин роста скорости взаимодействия при варьировании начального состава смеси можно рассматривать следующие факторы:
- Изменение скорости объемной генерации и концентрации атомов хлора. Этот механизм может реализоваться как при увеличении скорости диссоциации молекул Cl2 электронным ударом при изменении электрофизических параметров разряда, так и при появлении каналов ступенчатой диссоциации за счет взаимодействия с возбужденными частицами газов-добавок.
- Влияние состава смеси на кинетические характеристики гетерогенной рекомбинации атомов хлора.
- Влияние состава смеси на гетерогенные стадии взаимодействия активных частиц плазмы с обрабатываемым материалом.

|

|
Рис.1. Зависимость скорости травления Cu от доли аргона в исходной смеси Cl2/Ar (100 Па, 18 мА): 1 – 553 К; 2 – 573 К; 3 – 593 K |
Рис.2. Зависимости скоростей травления GaAs от начального состава смеси (100 Па, 18 мА, 373 К): 1 – Cl2/Ar; 2 – Cl2/N2 ; 3 – Cl2/H2 |
При исследовании параметров и механизмов плазмохимических процессов было найдено, что варьирование начального состава смесей Cl2/Ar, Cl2/N2, Cl2/O2 и Cl2/H2 при постоянных внешних параметрах разряда вызывает изменения электрофизических параметров плазмы, сопровождающиеся обогащением ФРЭЭ быстрыми электронами, ростом их средней энергии, скорости дрейфа и коэффициентов скоростей большинства пороговых элементарных процессов. В сочетании с изменением концентрации электронов в разряде для смесей Cl2/Ar и Сl2/N2 увеличение констант скоростей пороговых элементарных процессов представляет основной механизм влияния состава смеси на кинетику образования и гибели активных частиц. Процессы ступенчатой диссоциации молекул Cl2 при взаимодействии с метастабильными атомами Ar*(3p0,3p1,3p2), метастабильными N2*(A3Su+) и колебательно возбужденными N2*V>7 молекулами не эффективны из-за низких коэффициентов скоростей возбуждения и концентраций возбужденных частиц. В смесях Cl2/O2 и Cl2/H2 влияние начального состава смеси не ограничивается изменением электрофизических параметров плазмы, но сопровождается эффективной реализацией объемных атомно-молекулярных процессов. Так, в смеси Cl2/O2 реакция Cl2 + O(3P,1D) ® ClO + Cl вносит вклад, сравнимый со скоростью диссоциации Cl2 при электронном ударе и определяет вид зависимости концентрации атомов хлора от состава смеси. В смеси Cl2/H2 заметная роль в формировании стационарных концентраций частиц принадлежит реакциям H + HCl ® H2 + Cl (R1), H + Cl2 ® HCl + Cl (R2) и Cl + H2 ® HCl + H (R3). Скорости R2 и R3 взаимно компенсируются, однако скорость R1 при доле H2 в исходной смеси более 80% превышает скорость диссоциации Cl2 при электронном ударе. Для всех смесей предположение о постоянстве вероятности гетерогенной рекомбинации атомов обеспечивает удовлетворительное согласование расчетных и экспериментальных данных по приведенной напряженности электрического поля (E/N) и концентрации атомов хлора. Зависимость последнего параметра от состава смеси не является экстремальной (это подтверждается как при моделировании, так и при диагностике плазмы), что обеспечивает аналогичную монотонную зависимость плотности потока атомов хлора на поверхность подвергаемого травлению материала (рис. 3).
Анализ
представленных данных позволяет заключить, что изменение состава смеси не
обеспечивает немонотонного изменения кинетических характеристик образования
и/или гибели основных химически активных частиц, поэтому причину немонотонного
изменения скорости взаимодействия следует искать в изменении характеристик
гетерогенного взаимодействия. Анализ гетерогенной кинетики с использованием
адсорбционно-десорбционной модели плазменного травления показал, что появление
немонотонной зависимости скорости травления от состава смеси является возможным
в условиях ионно-стимулированного травления, когда доминирующим механизмом
очистки поверхности от продуктов травления является ионно-стимулированная
десорбция (![]() )
(рис. 4 – пример для смеси Cl2/Ar).
)
(рис. 4 – пример для смеси Cl2/Ar).
|
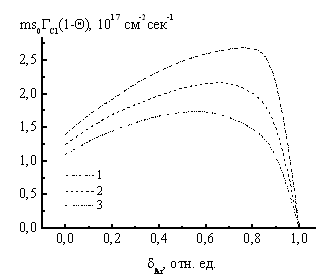
|
Рис.3. Расчетная
зависимость плотности потока атомов хлора на поверхность от состава исходной
смеси: 1 – Cl2/Ar;
2 – Cl2/N2; |
Рис. 4.
Прогнозируемая со-отношением (3.36) зависимость скорости взаимодействия от
начального состава смеси Cl2/Ar
(100 Па, 6.5×10-3 А/см2): |
Причиной
немонотонного поведения скорости травления служит конкуренция процессов
снижения потока химически активных частиц на поверхность и увеличения доли
чистой поверхности, в том числе - за счет активации десорбции продуктов при
ионной бомбардировке, вызванной ростом плотности потока ионов на поверхность. Высота
максимума и его положение на оси абсцисс определяются параметрами ![]() и
и ![]() , определяющими эффективность
заполнения и очистки активных центров продуктами взаимодействия.
, определяющими эффективность
заполнения и очистки активных центров продуктами взаимодействия.
В заключении раздела рассмотрим более подробно кинетические закономерности и особенности плазменного травления некоторых материалов, наиболее распространенных в технологии изделий электронной техники. Наибольший интерес здесь представляют:
- полупроводники Si и GaAs, являющиеся материалом подложек и основой создания активных элементов ИМС;
- диэлектрики SiO2 и Si3N4, используемые для изоляции элементов ИМС, пассивации структур, а также в качестве подзатворных диэлектриков при изготовлении МДП-транзисторов;
- металлы (Cu, Al, Сr, W, Mo), тонкие пленки которых формируют контакты и межэлементные соединения.
Арсенид галлия. Фториды галлия и мышьяка являются нелетучими соединениями, поэтому травление проводят в плазме хлорсодержащих газов Cl2, CCl2, BCl3, HCl, CCl2F2, Br2. Взаимодействие GaAs с молекулярным хлором в условиях газового травления отсутствует, основными химически активными частицами при травлении GaAs в плазме Cl2 являются атомы хлора. Влияние внешних параметров разряда (вкладываемая мощность, давление и расход газа) на скорость взаимодействия при постоянной температуре образца определяется изменением плотности потока атомов Cl на поверхность. При температуре 370 – 380 K происходит смена механизма взаимодействия от десорбции продуктов взаимодействия к химической реакции на поверхности, лимитируемой, в свою очередь, адсорбционно – десорбционными процессами. Основными проблемами при травлении арсенида галлия в хлорсодержащей плазме являются высокие скорости взаимодействия, переосаждение продуктов травления (и, как следствие, высокая шероховатость поверхности после травления), а также диспропорционирование химического состава поверхности из-за различной летучести хлоридов галлия и мышьяка. Альтернативой хлорсодержащим газам при травлении GaAs является водород. Скорость травления GaAs в плазме H2 значительно ниже, чем в плазме хлора, при этом наблюдается полирующее травление. Поэтому наиболее перспективными в настоящее время считаются смеси хлорсодержащих водородов, в которых регулирование состава смеси позволяет проводить процесс с приемлемыми скоростями и качеством (рис. 5).

а) |

б) |
Рис. 5. Влияние добавок водорода на морфологию поверхности GaAs после плазменного травления (500 Вт, 1.5 Па): а - CCl4; б - CCl4:H2 = 1:1.5 (по данным работы S. Semura, H.Saitoh Hydrogen mixing effect on reactive ion etching of GaAs in chlorine-containing gases // J. Vac. Sci. Technol. A(2), 1984, p. 474)
Кремний. Основные частицы, активные при травлении кремния –
атомы фтора и радикалы SF5
(исходные газы – CF4 или SF6), причем вклад последних в общую скорость травления
составляет около 30%. Скорость травления при всех условиях и составах плазмы
пропорциональна концентрации атомов фтора и увеличивается с ростом потока ионов
и разности потенциалов в системе «плазма-поверхность» при ![]() . При низких давлениях и частоте
поля, поддерживающего плазму, когда потенциал смещения образца относительно
плазмы велик и велики энергии ионов (~100 эВ), скорость
травления пропорциональна потоку ионов, что характерно для
ионно-стимулированного травления. Однако в плазме этот эффект вуалируется
другими эффектами – переосаждением распыляемых ионами электродов и стенок
реактора на поверхность образцов, высаживание твердых продуктов
плазмохимических реакций, полимеризация ненасыщенных углеродсодержащих
радикалов, - при этом скорость травления снижается. Такое же влияние оказывает
на скорость травления кремния окисление поверхности атомами кислорода.
Источником кислорода могут служить малые неконтролируемые примеси в
плазмообразующем газе, натекание атмосферы и др. Основной продукт травления в
газовой фазе - SiF4,
спонтанно испаряющийся с поверхности, и SiF2, удаляемый преимущественно при ионной бомбардировке
из-за высоких значений энергии десорбции. В хлорсодержащей плазме травление
протекает только по ионно-стимулированному механизму и характеризуется малыми
скоростями. Причина этого – диффузионные затруднения проникновения адсорбированных
атомов хлора в кристаллическую решетку кремния, поэтому в чисто химическом
процессе образуется труднолетучий SiCl2, обладающий хорошими маскирующими свойствами.
Основными химически активными частицами являются атомы хлора, при этом характер
зависимости скорости процесса от внешних параметров разряда сочетает признаки
химического (зависимость скорости взаимодействия от температуры подчиняется
закону Аррениуса) и ионного (нелинейная зависимость скорости взаимодействия от
тока разряда, снижение скорости с ростом давления газа) травления. При
травлении в хлорной плазме достигаются высокая анизотропия процесса и очень
высокие селективности травления кремния по отношению к SiO2.
. При низких давлениях и частоте
поля, поддерживающего плазму, когда потенциал смещения образца относительно
плазмы велик и велики энергии ионов (~100 эВ), скорость
травления пропорциональна потоку ионов, что характерно для
ионно-стимулированного травления. Однако в плазме этот эффект вуалируется
другими эффектами – переосаждением распыляемых ионами электродов и стенок
реактора на поверхность образцов, высаживание твердых продуктов
плазмохимических реакций, полимеризация ненасыщенных углеродсодержащих
радикалов, - при этом скорость травления снижается. Такое же влияние оказывает
на скорость травления кремния окисление поверхности атомами кислорода.
Источником кислорода могут служить малые неконтролируемые примеси в
плазмообразующем газе, натекание атмосферы и др. Основной продукт травления в
газовой фазе - SiF4,
спонтанно испаряющийся с поверхности, и SiF2, удаляемый преимущественно при ионной бомбардировке
из-за высоких значений энергии десорбции. В хлорсодержащей плазме травление
протекает только по ионно-стимулированному механизму и характеризуется малыми
скоростями. Причина этого – диффузионные затруднения проникновения адсорбированных
атомов хлора в кристаллическую решетку кремния, поэтому в чисто химическом
процессе образуется труднолетучий SiCl2, обладающий хорошими маскирующими свойствами.
Основными химически активными частицами являются атомы хлора, при этом характер
зависимости скорости процесса от внешних параметров разряда сочетает признаки
химического (зависимость скорости взаимодействия от температуры подчиняется
закону Аррениуса) и ионного (нелинейная зависимость скорости взаимодействия от
тока разряда, снижение скорости с ростом давления газа) травления. При
травлении в хлорной плазме достигаются высокая анизотропия процесса и очень
высокие селективности травления кремния по отношению к SiO2.
Оксиды кремния. Травление SiO2 осуществляется во фторсодержащей плазме атомами фтора и радикалами SF5 и CFx. При этом продуктами в газовой фазе являются SiF4, а также CO и SO, образующиеся при окислении радикалов кислородом, входящим в состав оксида. Поэтому эффекты полимеризации, переосаждения и пассивации в этой системе выражены гораздо слабее. При равных условиях процесса скорость травления SiO2 значительно ниже, чем непассивированного кремния, поэтому для этих материалов наблюдается высокая селективность травления.
Нитрид кремния. Как и оксид кремния, Si3N4 эффективно взаимодействует с атомами фтора и
фторсодержащими радикалами с выделением в газовую фазу SiF4 и N2.
Скорость травления в 8 – 10 раз меньше, чем у кремния. Положительное влияние на
скорость травления Si3N4
оказывают добавки к основному плазмообразующему газу углеводородов (CH4, C2H2, C2H4), приводящие к образованию легколетучего продукта NH3. При этом скорость травления нитрида кремния резко
возрастает, а самого кремния – снижается за счет пассивации его поверхности
полимерными пленками. В результате наблюдается обратное соотношение скоростей
травления: ![]() ~ 35 – 100.
~ 35 – 100.
Алюминий. Алюминий не имеет летучих галогенидов при комнатной температуре, за исключением Al2Cl6. Поэтому травление алюминия осуществляют в плазме хлорсодержащих газов (Cl2, CCl2, BCl3) и их смесей. Активными частицами, взаимодействующими с чистой поверхностью алюминия, являются как атомы, так и молекулы хлора. Вероятности их реакций при комнатной температуре одинаковы, ионная бомбардировка не ускоряет процесс. Скорость травления практически не зависит от величины отрицательного смещения на образце, а при травлении в хлоре и от мощности разряда. Последнее связано с тем, что увеличение степени диссоциации Cl2 с ростом вкладываемой мощности не приводит к существенному росту суммарной плотности потока ХАЧ на поверхность. Ситуация осложняется тем, что поверхность пленок алюминия легко окисляется атмосферным воздухом. Поэтому в технологии травятся, в основном, окисные пленки, травление которых обеспечивается атомами хлора в присутствии ионной бомбардировки. При преобладании химического механизма травления оно является изотропным, при этом анизотропия травления достигается двумя путями. Во-первых, это перераспределение вкладов механизмов травления в пользу ионного распыления, а также проведение процесса в условиях низких концентраций ХАЧ в газовой фазе (рис. 6). Во-вторых, анизотропное травление Al может быть достигнуто за счет добавки газов, генерирующих в плазме хлоруглеродные и бор-хлорные радикалы - CClx (x = 1-3) и BClx (x=1-2). Они осаждаются на поверхности, пассивируют ее и удаляются как и оксидные пленки при ионной бомбардировке. Продукты травления алюминия переосаждаются на стенках реактора и поверхности обрабатываемого материала, при этом, в силу их высокой гигроскопичности, возможно образование гидроксидов алюминия. Это приводит к невоспроизводимости результатов и к изменению свойств изделий, вплоть до полного стравливания участков пленки в воздушной среде даже под защитным покрытием. Поэтому необходим строгий контроль за примесью паров воды в газовой атмосфере реактора, а также меры по защите поверхности изделий после обработки, исключающие контакт алюминиевых слоев с воздушной средой.
|
а) б) |
Рис. 6. Структуры, получаемые при плазменном травления алюминия в хлоре: а- плазмохимическое травление, степень диссоциации Cl2 70% , б- реактивное ионное травление, степень диссоциации Cl2 30%. По данным работы: Samukawa S., Donnelly V. M. Effect of degree of dissociation on aluminum etching in high-density Cl2 plasma // Jpn. J. Appl. Phys. 37, 1998, p. L1036
Медь. Медные пленки травятся в хлорсодержащей плазме, поскольку хлориды меди более летучи, чем фториды. Медь взаимодействует как с атомарным, так и с молекулярным хлором, при этом скорости плазменного и газового (без разряда) травления меди в хлоре при одинаковых температурах образца различаются менее чем на 10%. Это свидетельствует о близких вероятностях взаимодействия для атомов и молекул Cl2. Для условий газового и плазменного травления, значения «эффективных» вероятностей взаимодействия составляют 1.7×10-2 и 2.1×10-2, соответственно (50 Па, 573 К). В области температур до 800 К основным продуктом взаимодействия на поверхности является Cu3Cl3, он же в газовой фазе при проведении газового травления и CuCl в газовой фазе при проведении плазменного процесса. При травлении в плазме хлора, в области температур 520 – 530 K происходит смена механизма травления от диффузии активных частиц в слое продуктов реакции и десорбции продуктов (Еа = 0.19±0.05 эВ) к химической реакции на поверхности, лимитируемой, в свою очередь, адсорбционно-десорбционными процессами (Еа = 0.85±0.05 эВ). Эти значения ниже как теплоты испарения продуктов реакции (1.6 эВ для Cu3Cl3 и 2.2 эВ для CuCl), так и энергии активации газового травления меди в хлоре, которая в интервале температур выше 500 К близка к теплоте испарения Cu3Cl3. Это указывает на дополнительную активацию десорбции в условиях плазменного травления при электронной и ионной бомбардировке образца. При Т > 500 K процесс плазменного травления протекает стационарно в кинетическом режиме и имеет первый кинетический порядок по концентрации химически активных частиц в газовой фазе.
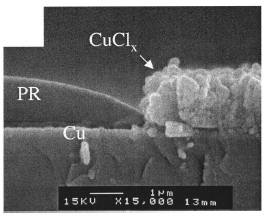
Основной технологической проблемой травления меди в хлорсодержащих газах является то, что для полного удаления продуктов реакции с поверхности при отсутствии иных стимулирующих факторов необходима температура порядка 250 0С (рис. 7). Поэтому развитие технологии травления идет по пути поиска таких факторов. Положительные результаты получены в плазменном процессе, активированном внешним УФ излучением с длиной волны 300 нм. Благодаря эффективной фотодесорбции продуктов реакции с поверхности процесс протекает в кинетическом режиме уже при комнатных температурах, а энергия активации травления в диапазоне температур 353 – 493 К составляет 0.12 эВ. В этих условиях абсолютная величина скорости травления достигает 400 нм/мин и линейно возрастает с ростом интенсивности УФ излучения.
а) |

б) |
Рис. 7. Морфология поверхности Cu после травления в плазме Cl2 (600 Вт, 20 мтор, 1 мин): а - 25 0С; б - 220 0С. По данным работы S. Lee, Y. Kuo Chlorine Plasma Copper Reaction in a New Copper Dry Etching Process // J. Electrochem. Soc.148(9), 2001, p. G524.
Еще одним новым направлением для снижения рабочей температуры является перевод хлоридов меди, образующихся в ходе газового травления, в соединения, обладающие высокой летучестью. Например, добавление в газовую среду триэтилфосфина (PEt3, Et = CH2CH3) в количестве 5% (об.) предотвращает полимеризацию CuCl в тримерную форму и сопровождается химической реакцией CuCl(s) + 2PEt3(g) ® ClCu(PEt3)2(g). Образующееся соединение ClCu(PEt3)2 обладает высокой термической устойчивостью (до 523 К), имеет высокое давление насыщенных паров (120 Па при 363 К) и является одним из самых летучих молекулярных соединений меди, известных в настоящее время. Это позволяет проводить газовое травление меди в среде Cl2 в кинетическом режиме, начиная с температур ~ 423 К, а характерные скорости травления при этой температуре составляют ~ 1 мкм/мин.
Хром. Травление хрома проводят в хлорсодержащей плазме, однако скорость процесса является очень низкой из-за низкой летучести образующихся хлоридов. Положительное влияние на скорость травления оказывают добавки кислорода, что приводит к образованию летучего оксихлорида хрома CrCl2O2. Согласно литературным данным, в смеси Cl2:O2=1:1 скорость травления достигает 18 нм/мин.
